Absorpsjon vs. adsorpsjon

Innhold
- Innhold: Forskjell mellom absorpsjon og adsorpsjon
- Hva er absorpsjon?
- Hva er adsorpsjon?
- Viktige forskjeller
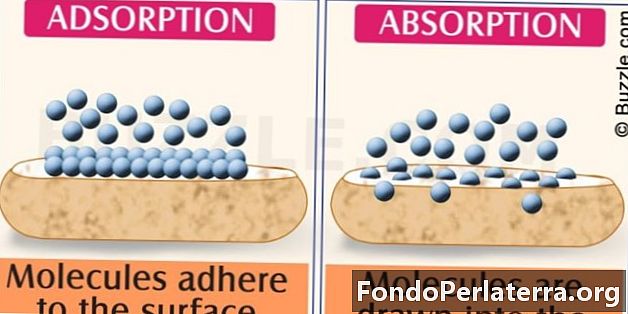
Hovedforskjellen mellom absorpsjon og adsorpsjon er, absorpsjon er prosessen der væske blir oppløst av enten fast stoff eller væske. Tvert imot, adsorpsjon er prosessen der ioner, molekyler eller atomer fra et stoff som gass, fast stoff eller væske, fester seg til overflaten av adsorbent.
Innhold: Forskjell mellom absorpsjon og adsorpsjon
- Hva er absorpsjon?
- Hva er adsorpsjon?
- Viktige forskjeller
- Videoforklaring
Hva er absorpsjon?
Absorpsjon er en prosess der ett stoff inngår i et annet stoff fullstendig. Det er en prosess der ett atom eller molekyl suges inni et volum av andre molekyler. Det må være en del av stoffet ved å gå helt inn i det. Det kan være en kjemisk eller fysisk prosess. For eksempel kan karbondioksid tas opp i kaliumkarbonatløsningen. Dette er et eksempel på kjemisk absorpsjon, siden en reaksjon finner sted. Et annet eksempel kan være å løse opp luft i vannet. Dette er fysisk absorpsjon siden luft kommer inn i vannet ved likevektstrykk. Når noe stoff eller materiale surrer inn en mengde væske eller gass inni, sies det at materialet har absorbert det andre materialet. Derfor, i absorpsjon, beveger det seg noe inne i et materiale.
Hva er adsorpsjon?
Adsorpsjon er prosessen der gass eller væske ikke absorberes, men den dannes bare over overflaten. Av syntetiske grunner og vannrensing er fenomenet adsorpsjon mye brukt i industrier. Det innebærer vedheft. Et stoff henger bare på det andre stoffet i denne prosessen uten å komme inn i det. For eksempel sitter karbondioksid på overflaten av adsorbent på innsiden av trykksvingningsadsorbentenhet. Den sitter på overflaten av fast adsorbent.
Viktige forskjeller
- Assimilering av molekylære arter gjennom hovedparten av faststoff eller væske betegnes som absorpsjon. Akkumulering av molekylære arter på overflaten og ikke kommer inn i den betegnes som adsorpsjon.
- Absorpsjon er et bulkfenomen mens adsorpsjon er et overflatefenomen.
- Absorpsjon er en endoterm prosess, mens adsorpsjon er en eksoterm prosess.
- Absorpsjon påvirkes ikke av temperatur, og adsorpsjon foretrekkes av lav temperatur.
- Absorpsjon skjer med jevn hastighet, mens adsorpsjonshastigheten øker jevnlig og når til slutt likevekt.
- Konsentrasjon er absorpsjon er den samme i hele materialet. Konsentrasjonen på overflaten er forskjellig i adsorpsjon enn den i bulk.
- Absorpsjon brukes kommersielt i kjølere og vannrensing.
- Absorpsjon er relatert til volum mens adsorpsjon er relatert til overflaten.
- Absorpsjon innebærer oppløsning og diffusjon mens adsorpsjon innebærer adhering.
- Ved absorpsjon blir energi fra et foton absorbert av en annen enhet.