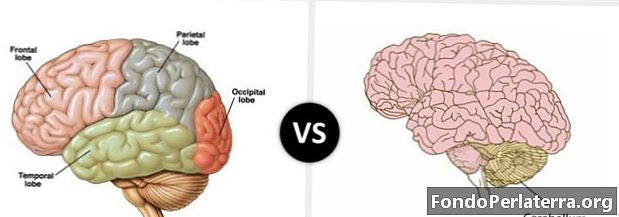
Varme vs. temperatur
Innhold
- Innhold: Forskjell mellom varme og temperatur
- Sammenligningstabell
- Hva er Heat?
- Hva er temperatur?
- Viktige forskjeller
Begrepet varme og temperatur analyseres sammen i matematikk, noe som er noe beslektet, men ikke likt. Begge begrepene er vanlige på grunn av deres brede bruk i vårt daglige liv. Det finnes en fin linje som avgrenser varme fra temperatur, i den forstand at varme er tenkt på, som en form for energi, men temperaturen er et mål på energi.
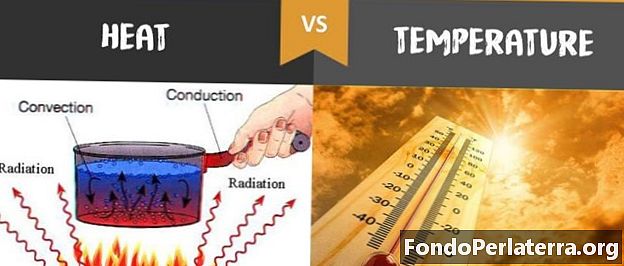
Hovedforskjellen mellom temperatur og varme er liten, men viktig, varme er den generelle energien i molekylbevegelsen, mens temperaturen er den gjennomsnittlige energien i molekylbevegelsen. Så la oss se på artikkelen gitt nedenfor, der vi har forenklet de to for deg.
Innhold: Forskjell mellom varme og temperatur
- Sammenligningstabell
- Hva er Heat?
- Hva er temperatur?
- Viktige forskjeller
- Videoforklaring
Sammenligningstabell
| BASIS | VARME | TEMPERATUR |
| Betydning | Varme er mengden energi i kroppen. | Temperatur er målet for varmeintensiteten. |
| Steps | Total kinetisk og potensiell energi inneholdt i molekyler i et objekt. | Den gjennomsnittlige kinetiske energien til molekyler i et materiale. |
| Eiendom | Flyter fra varmere objekt til kjøligere element. | Stiger når den blir oppvarmet og synker når den er avkjølt. |
| Arbeidsevne | Ja | Nei |
| Måleenhet | Joules | Kelvin |
| Apparater | calorimeter | Termometer |
| Merket som | Q | T |
Hva er Heat?
I fysikkvitenskap refererer varme til energien som overføres ved hjelp av arbeid eller annen materie. Generelt strømmer varmen fra et varmere objekt til et kaldere. Denne overføringen resulterer i en netto økning i entropi. Denne prosessen kan være direkte, som ved ledning og stråling, i tilfelle indirekte som i konvektiv sirkulasjon. Generelt refererer varme til prosessen med overføring mellom to systemer, systemene av interesse og omgivelsene som anses som et system, ikke en tilstand eller eiendom til et enkelt system. Mengden energi som overføres ved hjelp av varme uttrykkes i en SI-enhet av joule (J). Varme kan måles ved kalorimetri eller ved andre skaleringsteknikker som er basert på den første loven om termodynamikk. JR Partington - en britisk kjemiker - beskriver ledning som: “Hvis en varm kropp bringes i kontakt med en kald kropp, faller temperaturen på det varme kroppen og temperaturen i den kalde kroppen stiger, og det sies at en mengde varme ført fra den varme kroppen til den kalde kroppen. ”
Hva er temperatur?
I fysikk refererer temperatur til måling av varme eller kulde i et objekt ved bruk av et termometer. Ulike målestokker og foreninger brukes til å måle temperatur, som den vanligste blir brukt Celsius (betegnet med ° C og også kjent som celsius), Fahrenheit (betegnet med ° F) og i vitenskap med navnet Kelvin (betegnet med K). Temperatur er målet for gjennomsnittlig varme eller termisk energi til molekylene i et stoff. Når vi for eksempel sier at en objekttemperatur er 100 grader, betyr det ikke at hvert eneste molekyl har den nøyaktige termiske energien. I hvert stoff beveger molekyler seg med et annet spekter av energier, og samhandler med hverandre som endrer energiene. Temperatur er like viktig innen alle vitenskapsfelt som biologi, atmosfærisk vitenskap, fysikk, kjemi, geologi, medisin, kort sagt, i de fleste aspekter av dagliglivet.
Viktige forskjeller
- Varme refererer til mengden energi i et objekt, mens temperatur betyr måling av varme eller kulde i et objekt.
- Varme betegnes med symbolet ‘Q’ mens temperaturen betegnes med symbolet ‘T’.
- Systemen internasjonale (SI) varmeenhet er joule mens SI temperaturenhet er kelvin. Imidlertid brukes mange andre enheter som Celsius og Fahrenheit også for temperatur.
- Varme har muligheten til å utføre arbeidet mens temperaturen bare brukes til å måle varmegraden i et hvilket som helst stoff.
- Varme måles ved bruk av kalorimetri mens temperaturen måles med et termometer.
- Varme er målet for den totale kinetiske energien til alle molekyler i et stoff, mens temperaturen er målet for gjennomsnittlig kinetisk energi for molekyler i et stoff.
https://www.youtube.com/watch?v=AUGY9fOmuJY